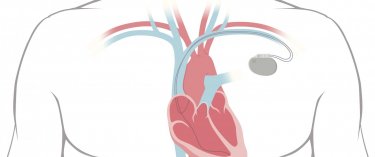
Implantation d’un stimulateur ou d’un défibrillateur cardiaque
Un certain nombre d’examens ont été réalisés et ont conduit à poser une indication de stimulation cardiaque définitive.
Pourquoi proposer l’implantation d’un stimulateur cardiaque ?
Cette décision est prise de façon collégiale en concertation avec le médecin ou le cardiologue traitant.
En temps normal, pour que le muscle cardiaque puisse se contracter, il existe un réseau de cellules électriques qui, en se dépolarisant, fait naître puis distribue le courant à l’ensemble du myocarde : c’est un peu « l’allumage » du coeur. Lorsque celui-ci est défaillant, le
coeur « cale ».
Il existe schématiquement deux types de troubles conductifs :
- Le premier est celui qui touche à la naissance même du courant électrique. Le coeur devient électriquement paresseux car le noeud sinusal d’où émerge le courant électrique, n’assure plus son rôle.
- Le deuxième est la non propagation de ce courant à l’ensemble du coeur.
De nombreuses raisons peuvent altérer le fonctionnement électrique du coeur. La plus fréquente est tout simplement le vieillissement. Avec le temps, les propriétés conductrices s’altèrent. Ce phénomène est normal mais ne touche pas l’ensemble de la population de façon égale. Ainsi, un patient pourra développer un trouble conductif à 60 ans alors qu’une autre personne plus âgée n’aura jamais de problème.
D’autre causes peuvent créer ou accélérer ces phénomènes. La principale cause « acquise » est l’infarctus du myocarde lorsqu’il touche le réseau électrique du coeur. Certains médicaments prescrits par le médecin peuvent aussi créer des troubles de la conduction électrique. Si la prescription est indispensable au bien-être, la mise en place d’un stimulateur cardiaque peut être indiquée afin de pouvoir poursuivre le traitement.
Plus rarement, certaines maladies du muscle cardiaque peuvent léser le réseau électrique cardiaque.
Lorsque des anomalies de la conduction électrique surviennent, il faut restaurer un fonctionnement normal du coeur. En l’état actuel de nos connaissances, il est impossible de réparer chirurgicalement le système électrique existant. De même, il n’existe pas de
médicament qui permet de faire mieux fonctionner un réseau défaillant sur le long terme. La seule possibilité thérapeutique est la mise en place d’une prothèse qui pallie le dysfonctionnement : c’est le stimulateur cardiaque.
Quand proposer l’implantation d’un défibrillateur cardiaque ?
La prévention primaire est une action prophylactique qui anticipe la survenue d’un évènement rythmique cardiaque potentiellement mortel. La maladie cardiaque entraîne un risque bien plus important que la population générale de présenter une mort subite. L’implantation d’un défibrillateur permettra en cas d’arythmie ventriculaire mortelle, de « ressusciter » le patient.
La prévention secondaire est une action réalisée a posteriori une fois la mort subite récupérée par l’équipe médicale. Il s’agira de traiter la récidive lorsqu’elle surviendra.
Ce sont les patients qui souffrent d’insuffisance cardiaque qui sont le plus souvent concernés par les troubles du rythme cardiaque mortels. C’est donc à eux que l’on propose le plus souvent la mise en place d’un défibrillateur. Plus rarement, certains troubles du rythme liés à une maladie génétique nécessitent également une implantation.
Comment est posé le diagnostic ?
Parfois, le diagnostic est évident.
Les symptômes sont typiques et correspondent à des anomalies électrocardiographiques ou structurelles du coeur. Dans ce cas, le cardiologue traitant, voire le médecin traitant, pose l’indication d’implantation du stimulateur ou d’un défibrillateur.
Dans d’autres cas, il existe des symptômes mais sans traduction électrocardiographique ou clinique évidente.
Le cardiologue réalise alors un bilan comprenant divers examens dont le but est de mettre en évidence des preuves électrocardiographiques ou structurelles. Il peut alors vous être proposé la pose d’un enregistreur électrocardiographique sur 24 ou 48h voire l’implantation d’un moniteur cardiaque. Au besoin une exploration électrophysiologique du coeur peut être réalisée en hospitalisation ambulatoire afin de mesurer précisément les temps de conduction intra-cardiaque.
-
Quel est le principe de fonctionnement du matériel ?
Un stimulateur ou un défibrillateur est composé de deux parties.
- La première partie est celle qui va générer l’impulsion électrique. C’est un boitier métallique hermétique en titane qui enferme la source d’énergie (pile lithium-ion) et le logiciel du stimulateur le dotant ainsi d’une intelligence artificielle. C’est cette partie que vous sentirez sous la peau. Lorsque le coeur se ralentit ou s’arrête de battre, le stimulateur en est informé par les mesures faites par la ou les sondes positionnées dans les cavités cardiaques. Il envoie alors des impulsions électriques qui entraine une contraction des cavités cardiaques à la fréquence programmée.
- La deuxième partie est celle qui va conduire l’électricité jusqu’au coeur : c’est la ou les sondes de stimulation. Ce n’est ni plus ni moins qu’un fils électrique qui stimule mais aussi écoute le coeur afin d’informer le boitier s’il doit ou non stimuler le coeur. C’est lors de l’implantation de la ou des sondes de stimulation que les éventuelles complications peuvent survenir.
Le défibrillateur a une fonction supplémentaire qui permet de générer une onde de choc entre la sonde ventriculaire et le boitier afin d’arrêter rapidement le trouble du rythme ventriculaire mortel.
-
Existe-t-il différents types de stimulateur ou défibrillateur cardiaque ?
On distingue 3 types de prothèses en fonction du nombre de sondes implantées dans les cavités cardiaques.
On peut stimuler :
- le haut du coeur (l’oreillette droite) ;
- le bas du coeur (ventricule droit et gauche) ;
- le haut et le bas du coeur.
Le choix de la prothèse dépend de l’indication d’implantation.
Comment implante-t-on le stimulateur cardiaque ?
L’implantation est un acte chirurgical et doit donc être réalisé sous stricte asepsie au bloc opératoire.
Cette intervention intéresse un organe vital en mouvement, elle doit donc être effectuée par un cardiologue spécialement formé à la rythmologie interventionnelle.
Une anesthésie locale est suffisante mais il est possible d’approfondir la sédation au besoin. Une consultation d’anesthésie est donc nécessaire avant l’implantation. Le stimulateur cardiaque peut être placé indifféremment à droite ou à gauche. Le choix dépend de l’habitude de l’opérateur, des conditions locales et des impératifs de chaque patient.
Après une petite incision sous la clavicule, une dissection chirurgicale permet d’implanter les sondes grâce au réseau veineux. Le positionnement précis des sondes dans les cavités cardiaques nécessite l’utilisation de rayons X. Les sondes sont vissées dans le muscle cardiaque puis des tests informatiques sont effectués en per-opératoire.
Le patient peut ressentir des palpitations pendant les tests. Une fois les sondes implantées, l’opérateur créé une loge entre la peau et le muscle pectoral afin d’y introduire le boitier connecté aux sondes de stimulation. C’est pour cette raison que le stimulateur cardiaque est visible sous la peau en dessous de la clavicule chez les patients maigres. Il faut compter entre 30 et 60 minutes pour l’ensemble de la procédure en fonction des conditions anatomiques.
Comment se déroule l’hospitalisation à l’Hôpital Américain de Paris?
-
L'admission
Votre admission est prévue 2 heures avant la procédure. Vous aurez réalisé auparavant la consultation d’anesthésie. Il faudra être à jeun depuis minuit la veille.
-
La préparation de l'intervention
Votre infirmier ou infirmière vous préparera pour l’intervention avec dépilation de la zone opératoire, mise en place d’une voie veineuse périphérique et réalisation de l’antibioprophylaxie péri-opératoire. Notre brancardier vous transportera jusqu’au bloc central 30 minutes avant la procédure.
-
Le bloc opératoire
Au bloc opératoire, votre panseur ou panseuse vous accueillera et vérifiera une nouvelle fois la complétude de votre dossier. Vous serez accueilli par votre anesthésiste et votre rythmologue. La durée de la procédure dépend des conditions anatomiques et du type de matériel implanté. Elle peut durer de 45 minutes à 2 heures.
-
L'intervention
Après l’intervention, vous serez dirigé vers la salle de soins postinterventionnelle
afin de vous réveiller en toute sécurité avant d’être transféré dans l’unité de soins intensifs cardiologiques pour 24 heures. Vous y bénéficierez d’une surveillance clinique permanente puisqu’un cardiologue est présent 24h/24. Une échographie cardiaque, une radiographie du thorax et une surveillance électrocardiographique seront réalisés par l’équipe. -
La durée d'hospitalisation
Votre hospitalisation ne dure, sauf complication, pas plus de 48 heures. Lors de votre sortie, l’ensemble des comptes rendus vous serons remis, ainsi que votre carte de porteur de stimulateur.
Comment se déroule le retour au domicile ?
Si vous travaillez, prévoyez 15 jours à 1 mois d’arrêt de travail. Vous ne pourrez pas pratiquer de sport pendant 30 jours, jusqu’à la consultation de contrôle qui a lieu 1 mois après l’intervention.
Un pansement hydrocolloïde vous sera apposé. Il faut le garder 7 jours puis le faire enlever par une infirmière à domicile grâce à l’ordonnance de sortie.
Une fois rentré chez vous, vous devez nous contacter :
- Si vous présentez de la fièvre et /ou une inflammation de votre cicatrice (purulente ou non) ;
- Si les symptômes ayant conduit à l’implantation récidivent ;
- Si la loge du stimulateur est douloureuse après avoir gonflé brutalement.
Il est très important que vous branchiez le transmetteur qui vous a été fourni sur la prise de courant dans votre chambre. Il doit rester posé sur votre table de nuit en permanence. Si vous quittez votre domicile plus de 15 jours, prenez votre transmetteur avec vous et branchez le dans votre nouvelle chambre.

Comment est contrôlé le bon fonctionnement du stimulateur ?
Il est indispensable de consulter régulièrement le rythmologue car lui seul peut contrôler l’entièreté du boîtier. Le rythmologue utilise un ordinateur qui permet de contrôler l’ensemble des paramètres du stimulateur ou du défibrillateur.
Il vérifie le bon fonctionnement du boîtier mais également celui du coeur sur le plan rythmique. En effet, celui-ci est pourvu d’une mémoire interne qui stocke en permanence toutes arythmies soutenues : être porteur de ce type de dispositif a donc un intérêt thérapeutique mais on l’oublie souvent, également un grand intérêt diagnostic. Cela permet une prise en charge précoce des arythmies et donc évite un retard thérapeutique aux conséquences graves dans certains cas.
Depuis quelques années, il est même possible de réaliser une grande partie du contrôle à distance par télécardiologie via un transmetteur fourni par le rythmologue. Cela améliore beaucoup la qualité de la surveillance tout en espaçant les consultations physiques.

Quelles sont les complications possibles ?
L’implantation d’un stimulateur ou d’un défibrillateur cardiaque n’est pas une chirurgie lourde. Les complications graves restent exceptionnelles.
Il ne faut cependant pas les ignorer car certaines peuvent avoir des conséquences graves si elles ne sont pas systématiquement recherchées.
L’ensemble des complications sont abordées lors des consultations préopératoires. Un consentement éclairé à signer est remis au patient afin de certifier qu’il a été informé des risques de l’intervention. Ce n’est en aucun cas une décharge de responsabilité.
-
Les douleurs post opératoires
Les douleurs post opératoires sont rares ou peu importantes. Un protocole systématique d’analgésie est prescrit après l’intervention.
-
Le déplacement d’une sonde de stimulation
Le déplacement d’une sonde de stimulation survient le plus souvent dans les jours qui suivent l’intervention. C’est pour cette raison que nous vous demandons de ne pas vous lever de la sortie du bloc opératoire au lendemain matin. Le diagnostic passe par la surveillance clinique, électrocardiographique et surtout radiologique. Repositionner une sonde est simple, rapide et indolore mais impose un retour au bloc opératoire.
-
L'hématome de la loge
La survenue d’un hématome de la loge est d’autant plus fréquente que le patient est sous antiagrégants plaquettaires voire sous anticoagulant à dose efficace.
Lorsque c’est possible, on peut interrompre ou baisser transitoirement ces traitements. Un pansement compressif est systématiquement mis en place après la procédure. Dans de rares cas, une évacuation chirurgicale de l’hématome est nécessaire si le patient ressent des douleurs ou si la suture est sous tension. -
L'épanchement de sang autour du coeur
La complication la plus grave est la survenue d’un épanchement de sang autour du coeur dans un espace habituellement virtuel entre le muscle cardiaque et le péricarde qui est un sac généralement collé au coeur.
Cette hémorragie interne est secondaire à la perforation du coeur lors de l’implantation des sondes. Le plus souvent, elle survient au niveau des oreillettes ou à la pointe du ventricule droit. Cette hémorragie évolue lentement et les signes cliniques peuvent être sournois au début. Il peut s’agir d’un manque de respiration, d’une pesanteur dans la poitrine ou d’un malaise général. C’est pour cette raison que nous réalisons systématiquement une échographie cardiaque de contrôle dans les suites de l’intervention. Comme tout syndrome hémorragique, cette complication est favorisée par la prise d’un traitement anticoagulant. La prise en charge consiste le plus souvent à une ponction per cutanée permettant d’évacuer l’épanchement de sang. Le recours à la chirurgie cardiaque reste très exceptionnel. -
Les troubles du rythme
Des troubles du rythme, le plus souvent auriculaire, peuvent survenir en post opératoire par irritation transitoire par la sonde.
Ces troubles du rythme sont plus fréquents chez les patients ayant déjà présenté ce type d’arythmie. Une majoration transitoire du traitement anti arythmique permet un retour rapide en rythme normal. -
Les contractions anormales au niveau du ventre
Des contractions anormales au niveau du ventre peuvent être dues à une stimulation du nerf phrénique par la sonde et les contractions du muscle pectoral à une fuite de courant au niveau des connecteurs.
Une reprogrammation du stimulateur suffit la plupart du temps à régler le problème. -
Le pneumothorax
Le pneumothorax est l’effraction de la plèvre lorsque le praticien ponctionne la veine sous clavière. L’espace virtuel entre la plèvre et le poumon se remplit d’air et le poumon se dégonfle comme un ballon de baudruche. Il devient inopérant et provoque un essoufflement du patient.
Le diagnostic est fait simplement sur la radiographie du thorax post opératoire. Le drainage de l’air par aspiration permet très rapidement au poumon de s’expandre et ainsi de retrouver son fonctionnement normal. Aucune séquelle secondaire n’est à craindre dans les suites. -
L’hémothorax
L’hémothorax est très exceptionnel et relève du même mécanisme que le pneumothorax. L’air est ici remplacé par du sang provenant le plus souvent d’une ponction accidentelle de l’artère sous clavière ou d’une fissuration du tronc veineux innominé.
-
Le syndrome septique
Il peut prendre plusieurs formes :
- En post opératoire immédiat, les signes classiques doivent être signalés tel que la fièvre, une rougeur voire un écoulement au niveau de la cicatrice.
- A distance de l’intervention, la prise en charge peut être retardée car le patient a quitté le milieu hospitalier. C’est pour cette raison que tout retard de cicatrisation doit être signalé au médecin traitant ou au centre implanteur. La consultation à 1 mois est pour cela un rendez-vous important à ne pas manquer. La survenue d’une infection impose, en plus d’un traitement antibiotique adapté au germe, le retrait de l’ensemble du matériel implanté.
Pour les patients porteurs d’un défibrillateur, la délivrance d’un choc électrique inapproprié doit être considérée comme une complication qui sera facilement traitée par une reprogrammation de la prothèse.
La prévention des infections nosocomiales est une priorité de santé publique. De nombreuses procédures existent dans la période per-opératoire afin de minimiser au maximum le risques.
Consultez nos cardiologues
En savoir plus